In Inorganic Syntheses mi sono imbattuto nella preparazione di un sale che avevo già provato a fare qualche anno fa, basandomi su un'altra fonte e con esiti allora abbastanza infelici.
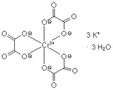
La sostanza in oggetto è formata dal catione potassio legato all'anione complesso del cromo con l'acido ossalico.
Ecco la "bruta" reazione sperimentale in gioco:
7 H2C2O4 + 2 K2CO3 + K2Cr2O7 --> 2 K3[Cr(C2O4)3] + 6 CO2 + H2O
Il cromo esavalente del bicromato viene ridotto a Cr(III) e complessato dall'ossalico; fortunatamente i coprodotti della reazione sono solo acqua e gas, quindi automaticamente separabili dal prodotto principale.
Ho cercato di rispettare per quanto possibile la stechiometria nei reagenti, in modo da avere alla fine (o almeno cercare di avere...) un prodotto accettabilmente puro.
Variando opportunamente (anche in maniera significativa) le procedure è possibile ottenere il medesimo tipo di sali complessi sostituendo il cromo con i metalli alluminio, ferro e cobalto, ottenendo triossaloalluminati, triossaloferrati e triossalocobaltati, con la formula generale [M(C204)3]3- , ognuno con tre molecole di acqua di cristallizzazione.
Nel nostro caso si otterrà alla fine K3[Cr(C2O4)3].3H2O
Materiale occorrente
Acido ossalico diidrato HOOC-COOH.2H2O
Potassio ossalato monoidrato KOOC-COOK.H2O
Potassio dicromato K2Cr2O7
-Ad una soluzione di 2,3 g di potassio ossalato monoidrato, di 5,5 g di acido ossalico diidrato in 80 ml di acqua, si aggiungono a piccole porzioni e mescolando vigorosamente, 1,9 g di potassio dicromato.
Si nota durante l'aggiunta il cambiamento di colore del bicromato da arancio a verdastro scuro e lo svolgimento di anidride carbonica.
Quando la reazione tende a finire, scaldare e poi evaporare fino ridurre il volume del lquido a circa un decimo di quello di partenza.
La fonte diceva di evaporare fin quasi a secchezza, ma vista l'esperienza precedente (principalmente al fine di non ottenere una polveraccia verdastra) ho preferito fermarmi prima per avere un prodotto ben cristallizzabile, al costo inevitabile di peggiorare la resa dal momento che il complesso è solubilissimo in acqua.
Lasciando raffreddare molto lentamente e poi una notte a riposare al freddo (di questa stagione ciò non costituisce un problema!) il potassio triossalocromato cristallizza in bei prismi di un verde scurissimo, quasi neri, dei quali ho purtroppo solo questa pessima immagine (che non rende alcuna giustizia al prodotto); le altre le ho perse.

La resa è stata scarsina come previsto, 4,5 g pari a circa il 67%, ma stavolta il risultato è stato indubbiamente migliore.
E così abbiamo fatto e visto anche questo complesso... ulteriore e semplice soddisfazioncina per chi ama la chimica sperimentale.

Inviato da: paoloalbert
il 02/05/2021 alle 21:53
Inviato da: Bepi1249
il 15/04/2021 alle 14:11
Inviato da: Tanner85
il 06/02/2021 alle 00:01
Inviato da: poetryclub
il 04/10/2020 alle 23:00
Inviato da: poetryclub
il 04/10/2020 alle 20:58