CHIMICA sperimentale
Esperienze in home-lab: considerazioni di chimica sperimentale e altro
Messaggi di Gennaio 2012
|
Post n°160 pubblicato il 29 Gennaio 2012 da paoloalbert
L'inverno è invece la sua stagione: ecco come si pavoneggia, re nella natura dormiente. |
|
Post n°159 pubblicato il 21 Gennaio 2012 da paoloalbert
Sembra una di quelle frasi al limite del paradosso, come quando si dice per ridere: -sai la differenza tra...?
(Per ritornare poi a questa pagina cliccare sull'immagine o sul nome del blog, in alto) |
|
Post n°158 pubblicato il 16 Gennaio 2012 da paoloalbert
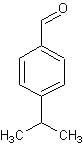
L'isopropilbenzaldeide, preparata, o meglio estratta, l'altra volta si presta perfettamente per un semplice e importante saggio della chimica organica analitica classica.
Ho eseguito la prova del saggio di Tollens sulla cuminaldeide usando un paio di ml di reattivo e una goccia di campione estratto.
Basta pochissima aldeide per far avvenire la reazione; ho provato con una frazione di goccia e la formazione dello specchio è ancora visibilissimo.
E' noto che il reattivo di Tollens va preparato al momento e non si può conservare perchè tende a formare, soprattutto in eccesso di ammoniaca e dopo reazioni intermedie, nitruro d'argento Ag3N. |
|
Post n°157 pubblicato il 10 Gennaio 2012 da paoloalbert
Qualcuno ha nell'orto il cumino? Il cumino è una pianticella erbacea di origine orientale della famiglia delle ombrellifere (come l'anice, il finocchio, il prezzemolo, ecc.) con dei piccoli semi oblunghi simili a quelli delle altre piante della famiglia. Solo due parole sull'uso di questa pianta: nella cucina indiana è uno degli ingredienti fondamentali del curry, mentre nella nostra gastronomia viene riservata perlopiù a preparazioni di "polveri" per insaporire le carni.
Ecco come ho proceduto per strappare a gran fatica quel poco di molecola odorosa che i piccoli semini cercavano di trattenersi con tutte le loro forze.
Nel nostro caso il vapore che si genera durante l'ebollizione è sufficiente a trascinare il prodotto in seno all'acqua che distilla (che infatti apparirà leggermente lattescente).
Il profumo non è proprio descrivibile, se non dire che è delicato ma molto speziato; insomma, sa proprio di... cumino!
Naturalmente il cumino contiene come al solito molte altre sostanze aromatiche oltre alla cuminaldeide, ma per la grande preponderanza che ha quest'ultima e per la procedura di estrazione, per i nostri scopi possiamo ritenere l'estratto come sufficientemente puro.
|
|
Post n°156 pubblicato il 02 Gennaio 2012 da paoloalbert
Anche questo è uno dei periodici intervallini, un po' diverso dal solito. Esisteva un tempo il Regno della STASI, una delle meno democratiche nazioni sulla faccia della Terra. Aveva (come il solito...) la parola "democratico" nel nome, e tanto basterebbe a renderla sospetta e sicuramente non confacente all'aggettivo. Ma aveva, quella Nazione, un inno nazionale meraviglioso, forse (per me) il più bello fra gli inni nazionali, capolavoro di Hanns Eisler; anche il testo (va ascoltato in tedesco!) è splendido. Ecco Auferstanden aus Ruinen:
|





 - macinare i semi di cumino in un mortaio; sono resistenti, ma insistere quanto basta fino a renderli una farina discretamente sottile. Questa operazione permette anche di pregustare ampiamente il buon profumo della
- macinare i semi di cumino in un mortaio; sono resistenti, ma insistere quanto basta fino a renderli una farina discretamente sottile. Questa operazione permette anche di pregustare ampiamente il buon profumo della  - mettere i semi macinati assieme a 400 ml d'acqua in un pallone da 500 ml e predisporre per la distillazione con refrigerante Liebig e relativi accessori.
- mettere i semi macinati assieme a 400 ml d'acqua in un pallone da 500 ml e predisporre per la distillazione con refrigerante Liebig e relativi accessori.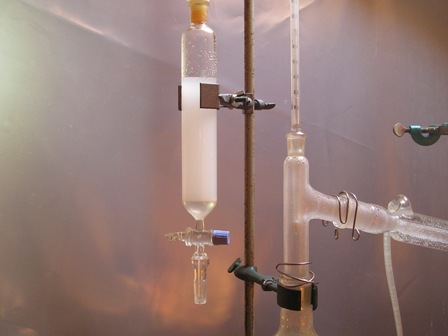 - porre il liquido distillato in un imbuto separatore ed estrarre con almeno 5/6 porzioni da 10 ml ciascuna di
- porre il liquido distillato in un imbuto separatore ed estrarre con almeno 5/6 porzioni da 10 ml ciascuna di 
Inviato da: paoloalbert
il 02/05/2021 alle 21:53
Inviato da: Bepi1249
il 15/04/2021 alle 14:11
Inviato da: Tanner85
il 06/02/2021 alle 00:01
Inviato da: poetryclub
il 04/10/2020 alle 23:00
Inviato da: poetryclub
il 04/10/2020 alle 20:58