CHIMICA sperimentale
Esperienze in home-lab: considerazioni di chimica sperimentale e altro
Messaggi di Luglio 2013
|
Post n°240 pubblicato il 18 Luglio 2013 da paoloalbert
Agli esordi di questo blog avevo presentato una bella pianticella di Datura stramonium; era un periodo in cui questi tossici e interessanti vegetali si erano chissà come diffusi in un campo ex coltivato a mais vicino alla mia zona.
Ora, nell'attesa dei frutti e dei semi, godiamoci questa fresca e come sempre meravigliosa estate.
|
|
Post n°239 pubblicato il 08 Luglio 2013 da paoloalbert
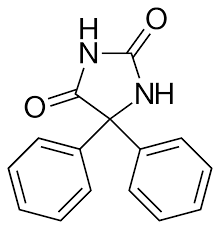
E siamo arrivati così al terzo e ultimo passaggio: partendo dalla benzaldeide si arriva al benzoino, dal benzoino al benzile e oggi dal benzile alla fenitoina, con l'unico scopo (chiaro e fondamentale in tutto il mio blog) di giocare con le molecole.
Mi mancano purtroppo stavolta le immagini della sintesi. Porre con refrigerante a ricadere a riflusso per circa cinque ore. Alla fine raffreddare in ghiaccio e filtrare la piccola quantità di precipitato giallo che si è formato, parte del quale aderisce alle pareti del pallone. [Secondo la mia fonte dovrebbe essere difenilacetilene diureide...(?). Sarebbe molto interessante ottenere qualche notizia in merito anche a queste reazioni secondarie, ma sarà ben difficile reperirle] Aggiungere al filtrato circa 100 ml di acqua e acidificare la soluzione con HCl fino a pH leggermente acido (4-5). Acidificando precipiterà la fenitoina grezza, in fogliette leggere di colore nocciola chiaro. Raffreddare in ghiaccio e filtrare spremendo bene, indi lavare con acqua fredda. Ho verificato che sarebbe possibile decolorare perfettamente la fenitoina per mezzo di una piccola quantità di carbone attivo; non ho effettuato l'operazione avendone in gioco solo poco più di un grammo ma sicuramente ne varrebbe la pena avendone di più e volendo ottenere un prodotto perfettamente bianco. Infine ecco la 5,5-difenilidantoina (fenitoina) che è il prodotto ottenuto.
|



Inviato da: paoloalbert
il 02/05/2021 alle 21:53
Inviato da: Bepi1249
il 15/04/2021 alle 14:11
Inviato da: Tanner85
il 06/02/2021 alle 00:01
Inviato da: poetryclub
il 04/10/2020 alle 23:00
Inviato da: poetryclub
il 04/10/2020 alle 20:58