CHIMICA sperimentale
Esperienze in home-lab: considerazioni di chimica sperimentale e altro
Messaggi di Febbraio 2012
|
Post n°166 pubblicato il 29 Febbraio 2012 da paoloalbert
Guardate cosa m'ha regalato la gentile signorina Flavia per il mio compleanno: un bel filetto di platino nuovo!
Il filo nel suo "fodero" - Il filo pulito nella fiamma: nessuna colorazione
Il filo con una traccia di SrBr2: l'inconfondibile rosso dello stronzio |
|
Post n°165 pubblicato il 21 Febbraio 2012 da paoloalbert
Sul sito di Rosalba (Crescere Creativamente) è ospitato il quattordicesimo Carnevale della Chimica, che ha come tema "La chimica delle nascite", da interpretarsi naturalmente in senso libero. Dopo un po' nel bicchiere nuoterà una sgradevole torbidità marrone, che, agli occhi... degli allocchi sarà la prova inconfutabile che l'acqua, inizialmente bella, limpida e pulita, in realtà nascondeva chissà quali porcherie, abilmente tenute nascoste da quel cattivone del proprio Comune.
|
|
Post n°164 pubblicato il 20 Febbraio 2012 da paoloalbert
Ed eccoci a Pietrapertosa, sotto la neve, dall'unico posto in cui ho potuto fotografare un frammento di paese; impossibile fare quello che s'avea da fare in questa località (calpestare un po' di Dolomiti Lucane), ma visto il periodo basta essere riusciti ad arrivare... |
|
Post n°163 pubblicato il 15 Febbraio 2012 da paoloalbert
Visto il periodo favorevole (inverno...), il clima ideale (un freddo boia...), le precipitazioni scarse (mezza Italia sotto la neve...), le strade percorribili (con la motoslitta...), ce ne andiamo qualche giorno a fare i turisti in questa zona:
|
|
Post n°162 pubblicato il 08 Febbraio 2012 da paoloalbert
Oggi un grado sottozero nel mio lab, e un paio di notti fa meno quattordici fuori, là dove c'è il noce.
|
|
Post n°161 pubblicato il 03 Febbraio 2012 da paoloalbert
Visto il mio vecchio noce commentato in atmosfera invernale, l'amico Marco mi invita, credo scherzosamente, a meditare sull'estrazione dello juglone dai malli delle noci. Non è per niente una cattiva idea... ma ho già fatto questo lavoretto! L'ho fatto in maniera poco chimica in verità, tant'è che il recipiente ultimo di reazione non è un pallone o una beuta ma una affusolata bottiglietta dove il prodotto, o meglio quello che ne resta, si trova più a suo agio. Ecco qui sotto, fra i rami di un nocello giovane e ora spoglio che a suo tempo mi ha fornito i frutti, la sperimentale estrazione che ho fatto l'altr'anno.  Ne era venuto un nocino da fine del mondo, messo in cantiere come si deve proprio il giorno di San Giovanni, perchè non si dica poi che non si è fatto tutto in regola. Per un chimico le prove organolettiche sono ancor più di soddisfazione rispetto a un comune mortale; per esempio vengono assurdi pensieri come: -guarda che bel colore ambrato sempre più scuro che conferisce questo juglone (che è un naftochinone) al nocino che invecchia! -anche la catechina (un flavanolo) contribuisce all'aspetto, ma quanto? -che sia sovrastante il suo colore o il suo gusto astringente? -non par di sentire, all'assaggio attento, quella "legatura" tannica dell'acido gallico? -ma che gusto questa deliziosa mix di polifenoli! ... e così via ragionando... discorsi da fuori di testa dirà qualcuno al quale la chimica sta leggermente indigesta. Tornando in ambito chimico, ho visto girovagando in rete un bel lavoro sloveno proprio sull'estrazione dei polifenoli dallo Juglans regia, ovvero dal nostrano pregiato noce bianco. Il contenuto in juglone è abbastanza elevato (una quindicina di mg per grammo di noce verde), ma la separazione del medesimo da tutto l'estratto (il quale si può fare comodamente con i primi due alcoli), non è certo facilmente fattibile, o almeno non lo è con i miei mezzi. L'estratto di noce verde, che in definitiva non è altro che un "nocino" non zuccherato e non aromatizzato, contiene una bella serie di polifenoli (in genere sotto forma di glicosidi), tutte sostanze fortemente antiossidanti. Eccoli qui: 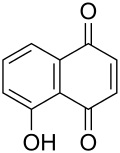 Juglone (relativamente tossico, 5-idrossinaftochinone 15 mg/g) 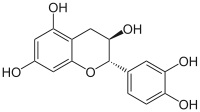 Catechina (colorante, astringente, 0,15 mg/g) 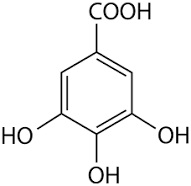 Acido gallico (3,4,5-triidrossibenzoico, astringente, 0,7 mg/g) 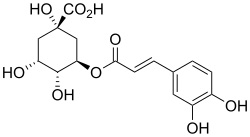 Acido clorogenico (un estere dell'acido 3,4-diidrossicinnamico, 0,05 mg/g) 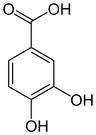 Acido protocatechico (3,4-diidrossibenzoico, 1 mg/g) Quando bevete un vero nocino modenese, siete avvertiti voi allergici alla chimica! |













Inviato da: paoloalbert
il 02/05/2021 alle 21:53
Inviato da: Bepi1249
il 15/04/2021 alle 14:11
Inviato da: Tanner85
il 06/02/2021 alle 00:01
Inviato da: poetryclub
il 04/10/2020 alle 23:00
Inviato da: poetryclub
il 04/10/2020 alle 20:58