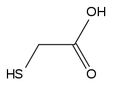
Con molta fatica ho trovato in giro una sintesi (incompleta) di questo acido un po' insolito e ho voluto provarla adattandola come mi sembrava opportuno; avevo inoltre a disposizione un piccolo residuo di acido monocloroacetico CH2Cl-COOH da sacrificare a maggior gloria (il gruppo -SH mi è molto più simpatico di un banale -Cl)... quindi... mano alle beute!
Materiale occorrente:
- acido monocloroacetico
- sodio idrossido
- sodio tiosolfato
- acido cloridrico
- etere
- vetreria opportuna
- In una beuta da 100 ml neutralizzare 5 g di acido monocloroacetico CH2Cl-COOH con 2,2 g di NaOH sciolti in 15 ml di acqua; aggiungere poi 9 g di sodio tiosolfato Na2S2O3 in 35 ml di acqua, e riscaldare per un'ora in bagno d'acqua bollente.
Un campione non deve diventare torbido (sep. di S) per acidificazione.
Idrolizzare poi la miscela con 10 ml HCl al 25% riscaldando sempre per un'ora su bagno d'acqua.
Alla fine lasciar raffreddare ed estrarre l'acido mercaptoacetico (che è solubile anche in acqua, quindi se ne perde purtroppo una discreta quantità) con due porzioni da 25 ml di etere cadauna, unite poi insieme.
Lasciar evaporare l'etere (no fiamme in giro! ambiente adatto!) e raccogliere il poco HS-CH2-COOH che si è formato e che siamo riusciti ad estrarre.
Avendone una quantità decente si può purificare per successiva distillazione in vuoto (cosa che ovviamente non ho fatto). - p.e. 125° a 30 mmHg, d. 1,3 -
L'acido mercaptoacetico (qualcuno lo chiama anche tioglicolico) si presenta come un liquido incoloro che presto diventa giallino, con un odore particolare sgradevole, come è logico che sia visto il gruppo -SH che si ritrova attaccato alla testa.
Industrialmente quest'acido serve per delle preparazioni riguardo le "permanenti" delle signore, poichè sotto forma di sale d'ammonio interagisce con i ponti disolfuro della cheratina dei capelli; il suo sale di calcio serve invece come depilatore nell'industria delle pelli.
A me è servito, oltre che per la fondamentale curiosità e divertimento nella sintesi, per un bel saggio dello ione ferro che metterò prossimamente su questo schermo... pardon, su questo blog, in un post a lui tutto dedicato.

Ecco il prodotto frutto della fatica di oggi, dove al posto di un idrogeno metilico dell'acido acetico c'è un bel gruppo -SH; è solo un misero fondo di provetta, ma il resto è riempito dalla soddisfazione!

Inviato da: paoloalbert
il 02/05/2021 alle 21:53
Inviato da: Bepi1249
il 15/04/2021 alle 14:11
Inviato da: Tanner85
il 06/02/2021 alle 00:01
Inviato da: poetryclub
il 04/10/2020 alle 23:00
Inviato da: poetryclub
il 04/10/2020 alle 20:58