CHIMICA sperimentale
Esperienze in home-lab: considerazioni di chimica sperimentale e altro
| « Guerra chimica e puzzole! | Arsenico e vecchi... pallini » |
|
Post n°20 pubblicato il 11 Marzo 2010 da paoloalbert
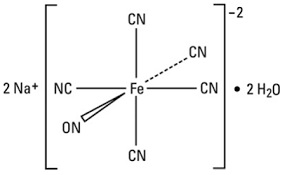
Un interessante metodo di analisi per via umida dei solfuri è quello che prevede l'uso del nitroprussiato sodico. Questo sale cianonitrosilico del ferro forma con lo ione solfuro un complesso di coordinazione rosso-violetto di grande potere colorante, grazie al quale la reazione si dimostra sensibilissima. K4[Fe(CN)6] + 6 HNO3 = H2[(NO)Fe(CN)5] + 4 KNO3 + NH4NO3 + CO2 H2[(NO)Fe(CN)5] + Na2CO3 = Na2[(NO)Fe(CN)5] + H2O + CO2 Materiali occorrenti: In un beaker da 400 ml sciogliere 40 g di K4[Fe(CN)6]•3H2O in 60 ml di acqua tiepida. Aggiungere poi agitando 64 ml di HNO3 al 40%. Tenere la miscela in bagno di acqua tiepida finchè una goccia test della sol. bruna reagisce con una sol. di FeSO4 dando un precipitato verde scuro e non blù.
Il nitroprussiato è molto velenoso, ma trova utilità in medicina come terapia d'emergenza nell'ipertensione grave perchè riduce drasticamente e velocemente la pressione sanguigna. Per l'analisi dei solfuri ho preparato per diluizioni successive quattro soluzioni, contenenti rispettivamente 100, 30, 10, 3 ppm di sodio solfuro in acqua.
|
https://blog.libero.it/paoloalbert/trackback.php?msg=8547440
I blog che hanno inviato un Trackback a questo messaggio:
MENU
ULTIMI COMMENTI
Inviato da: paoloalbert
il 02/05/2021 alle 21:53
Inviato da: Bepi1249
il 15/04/2021 alle 14:11
Inviato da: Tanner85
il 06/02/2021 alle 00:01
Inviato da: poetryclub
il 04/10/2020 alle 23:00
Inviato da: poetryclub
il 04/10/2020 alle 20:58