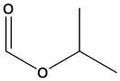
Un volonteroso giovane sperimentatore mi ha chiesto qualche consiglio riguardo la sintesi del formiato di isopropile.
Le sintesi degli esteri secondo Fischer sono un'ottima palestra per impratichirsi con la chimica sperimentale organica per molti motivi: sono procedure quasi sempre facili, hanno una buona resa, fanno imparare a distillare, frazionare, purificare, misurare il punto di ebollizione (ed è già tanto!) e, dulcis in fundo, conducono generalmente a dei simpaticissimi prodotti profumati i cui termini inferiori sono detti, più o meno a ragione, "esteri di frutta".
Naturalmente il formiato di isopropile non manca nella mia piccola collezione, avendolo a suo tempo prodotto specificamente per sentirne il profumo (o l'odore, dipende dai punti di vista).
Fotografie questa volta non ne metto perchè non aggiungerebbero nulla di nuovo agli analoghi post precedenti.
Materiali occorrenti:
-Acido formico
-Isopropanolo
-Acido solforico
-Vetreria opportuna
Reazione semplificata
H+
CH3-CH(CH3)-OH + H-COOH ----> H-COO-CH(CH3)-CH3 + H2O
In un pallone da 250 ml si intoducono 48 g (40 ml) di acido formico all'85% e 32 g (40 ml) di alcool isopropilico; poi cautamente mescolando si aggiungono 4 ml di H2SO4 conc.
Ho usato un deciso eccesso di HCOOH sia perchè è all'85% ma soprattutto per spostare l'equilibrio verso la formazione dell'estere.
Nella Fischer non si usano mai le quantità stechiometriche dei due reagenti ma sempre un eccesso del reagente che più conviene, o dal punto di vista economico o da quello chimico-fisico; in questo caso ho privilegiato l'acido perchè il suo azeotropo con l'acqua ha un p.eb. più elevato di quello tra l'isopropanolo e l'estere formico (abbastanza vicini), in modo da avere alla fine meno alcol residuo.
Organizzare il sistema con riscaldamento e refrigerante a ricadere e portare il pallone all'ebollizione e a lento riflusso per circa un'ora.
Alla fine sostituire l'Allhin con un refrigerante Liebig e distillare raccogliendo tutto ciò che passa fino a 95° circa.
Versare il distillato in un imbuto separatore e neutralizzarlo con la sufficiente quantità di sol. satura di NaHCO3 (o magari anche un po' di solido), agitando bene fino a cessato sviluppo di CO2; ne serve una buona quantità perchè parecchio ac. formico non reagito è passato nel distillato.
Ripetere un paio di volte l'operazione fino a neutralizzazione completa e lavare bene con acqua, separando ogni volta la fase acquosa sottostante (l'estere ha d. 0,87).
Essicare il prodotto con CaCl2 o altro disidratante e ridistillare, raccogliendo ciò che passa intorno ai 70°.
La resa è stata 43 ml (37 g), circa il 75%.
Come si può vedere la sintesi è facilissima, semplice e lineare nelle due distillazioni e con resa quasi teorica nel rapporto acido/alcool usato.
Pur facendo parte della "famiglia" degli esteri di frutta (intendo gli esteri degli alcoli e acidi grassi inferiori), il formiato di isopropile non è da considerarsi un degno rappresentante di questa famiglia, perchè il suo odore non è per niente fruttato ma solo etereo con un fondo pungente, come generalmente gli altri formiati.
Inviato da: paoloalbert
il 02/05/2021 alle 21:53
Inviato da: Bepi1249
il 15/04/2021 alle 14:11
Inviato da: Tanner85
il 06/02/2021 alle 00:01
Inviato da: poetryclub
il 04/10/2020 alle 23:00
Inviato da: poetryclub
il 04/10/2020 alle 20:58