
Fra i molti metodi di ricerca analitica del rame c'è una curiosa e tanto sensibile procedura, che perfino il Treadwell (la Bibbia della chimica analitica classica) afferma: "...è questa una reazione troppo sensibile per le normali ricerche analitiche"!
Di cosa si tratta? L'ho recentemente risperimentata e val la pena di raccontarla.
Il metodo si basa sul fatto che lo ione ferrico Fe(III) reagisce con il sodio tiosolfato Na2S2O3 generando una colorazione violetta che sparisce al termine della reazione di riduzione per la formazione di ione tetrationato incoloro; complessivamente la reazione è la seguente:
2 Fe+++ + 2 S2O3-- --> 2 Fe++ + S4O6--
Il trucco è che il rame, anche se presente in tracce minime, accelera enormemente questa reazione per effetto catalitico.
Se si opera in presenza di ione tiocianato -CNS si ottengono due vantaggi:
- si riconosce nettamente la fine della reazione dalla scomparsa della colorazione rossa del tiocianato ferrico Fe(CNS)3
- si rende molto lenta la reazione in assenza di rame perchè il tiocianato ferrico è pochissimo dissociato e la concentrazione di ioni ferrici in soluzione è piccolissima e pertanto la riduzione da Fe(III) a Fe(II) è molto lenta.
Dopo questa doverosa introduzione, indispensabile per capire tutto l'interessante meccanismo, vediamo la fase operativa:
Oggi lo chef va a preparare due soluzioni:
- 0,1 g di sodio tiosolfato Na2S2O3 in 10 ml di acqua distillata
- in altrettanti 10 ml di acqua sciogliere 0,15 g di cloruro ferrico FeCl3.6H2O e 0,2 g di ammonio tiocianato NH4CNS
La seconda soluzione assume ovviamente una intensissima colorazione rossa (appare quasi nera data l'intensità cromatica elevatissima del tiocianato ferrico).
Esecuzione del test:
- Porre in due incavi di una piastrina di porcellana una goccia della soluzione in esame contenente rame e una goccia d'acqua distillata.
- A ciascuna delle due gocce si aggiunge una goccia della sol. di tiocianato ferrico e due-tre goccie della sol. di tiosolfato, mescolando immediatamente con due bacchettine di vetro (non la stessa!).
- In assenza di rame (prova in bianco) si ha decolorazione dopo 1-2 minuti, in presenza di rame la decolorazione è immediata.
Ho voluto vedere dove arriva la sensibilità, preparando per diluizioni successive una soluzione di solfato di rame contenente alla fine 5 ppm (!!) di Cu++ .
Poi non ho più diluito, altrimenti rimaneva solo acqua...
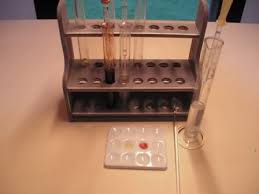
L'unica fotografia (eseguita in una pessima e scura giornata) lascia all'immaginazione risultato: comunque nei pozzetti di destra c'è la prova in bianco, a sinistra quelli contenenti la traccia di rame, il tutto fotografato dopo una decina di secondi; la decolorazione dove c'erano tracce di Cu è avvenuta quasi istantaneamente.
(Non si vede, ma credetemi sulla parola...).
L'effetto catalitico è dato, oltre che dal rame, anche dall'arsenico, che in questa occasione non ho provato.

Inviato da: paoloalbert
il 02/05/2021 alle 21:53
Inviato da: Bepi1249
il 15/04/2021 alle 14:11
Inviato da: Tanner85
il 06/02/2021 alle 00:01
Inviato da: poetryclub
il 04/10/2020 alle 23:00
Inviato da: poetryclub
il 04/10/2020 alle 20:58