Prima della pausa natalizia voglio completare la trilogia degli esteri benzilici degli acidi grassi inferiori, proponendo la terza e ultima sintesi di un altro estere odoroso importante, quella del formiato.
Il metodo è sempre Fischer e ricalca quella dell'acetato (al quale rimando per confronto); non avendo a disposizione acido formico anidro ma solo all'85%, ho usato un grande eccesso di quest'ultimo (circa 1:4) per essere quasi sicuro di salificare tutto l'alcool e non trovarmelo poi come residuo.
Occorre anche questa volta armarsi di pazienza per i lunghi tempi di ebollizione a ricadere ed i successivi lavaggi.
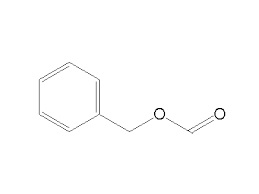
Materiale occorrente:
- alcool benzilico C6H5-CH2-OH
- acido formico 85% H-COOH
- acido solforico H2SO4
- sodio bicarbonato NaHCO3
- refrigerante allhin
- vetreria varia
- In un pallone da 250 ml introdurre 28 ml di alcool benzilico e 46 ml di acido formico all'85%; mescolando aggiungere 2 ml di H2SO4 conc. e predisporre il sistema per riscaldamento a ricadere con mantello riscaldante o con bagno ad olio o sabbia. Ho usato questo sistema, immergendo nella sabbia il termometro.
Portare ad ebollizione e tenere a lento riflusso per circa sei-sette ore, con la temperatura che si assesta mediamente sui 190-200°.
Alla fine del tempo versare la miscela in 200 ml di acqua e mescolare, si forma un'emulsione bianca difficilmente separabile, quindi lasciar riposare una notte.
Dopo la separazione, decantare cautamente il liquido sovrastante (va via la maggior parte dell'abbondante acidità residua), aggiungere 100 ml di una soluzione satura di NaHCO3 e mescolare fino a sicura e completa neutralizzazione. Eventualmente insistere in questo particolare. Lasciar ancora separare (questa volta è molto più veloce) e lavare bene un altro paio di volte con acqua, sempre con le pause opportune per la separazione delle fasi a piccola differenza di densità.
Come detto, la procedura di lavaggio è lunga ma evita di dover estrarre con solvente (CCl4 o etere) e poi separare a sua volta l'estere dal solvente.
Alla fine separare dall'ultima acqua con imbuto separatore e seccare con 5 g di CaCl2. Si deve ottenere un liquido perfettamente limpido (se contiene umidità è sempre lattiginoso).
Distillare il prodotto (circa 30 ml) raccogliendo tra 200 e 208°,ottenendo 17 ml di benzile formiato (64%).
Il residuo della distillazione, più altobollente e leggermente giallino, ha quasi identico profumo.
D. 1,05 - P.e. 203°- Liquido limpido incoloro, oleoso (un po' contro la logica?), con odore fruttato, diciamo una via di mezzo tra il gelsomino e le mandorle, ma più debole e aspro, meno gradevole e diverso dal benzilacetato o propionato.
Il benzilformiato si trova in natura in piccola quantità solo nel mirtillo rosso.

Sarebbe interessante conoscerne l'effettiva purezza, per verificare la presenza di eventuali prodotti di ossidazione e/o reazioni secondarie... ma ci vorrebbe "un apparecchio con la spina!".


Inviato da: paoloalbert
il 02/05/2021 alle 21:53
Inviato da: Bepi1249
il 15/04/2021 alle 14:11
Inviato da: Tanner85
il 06/02/2021 alle 00:01
Inviato da: poetryclub
il 04/10/2020 alle 23:00
Inviato da: poetryclub
il 04/10/2020 alle 20:58