Parafrasando al plurale la celebre frase di Don Abbondio, cosa sono questi acidi carbossilici?
E perchè questa domanda?
Semplicemente perchè il discorso di oggi non è dedicato ai chimici ma... ai passanti!
Non sono infinite le vie del Signore? E allora non potrebbe capitare che qualche anima dispersa passando di qui per caso abbia il coraggio di mettersi a leggere qualche riga di quello che dico, magari avendo sentito nominare questi acidi in maniera estemporanea?
I chimici quindi per oggi possono farsi un giretto...
________________________
Passante, ti è chiara innanzitutto la differenza tra Chimica Organica e Chimica Inorganica?
La chimica inorganica tratta di tutti i 92 elementi della natura e dei relativamente pochi loro composti, la Chimica Organica tratta solo del carbonio e dei suoi milioni di composti.
Come è possibile questo paradosso? Novantadue ne fanno pochi e uno solo ne fa milioni? Per ora prendiamo per buona questa singolare affermazione e accettiamola per vera (come in realtà è).
Intanto c'è da dire che gli acidi carbossilici fanno parte della chimica organica e quindi per forza devono contenere il carbonio.
Altro apparente paradosso: il carbonio si lega solo con pochi altri elementi per dare origine alla sua prolificissima milionaria famiglia e fra questi pochi preferiti ci sono solo l'idrogeno, l'ossigeno e l'azoto. (Spesso, e di enorme importanza soprattutto in biochimica, c'è anche qualche altro invitato speciale, come il fosforo, lo zolfo ed altri, ma la stragrande maggioranza dei composti organici del carbonio è fatto solo di idrogeno, ossigeno e azoto, spesso nemmeno insieme).
L'atomo di carbonio forma dei legami (e qui ci vuole un provvidenziale omissis...) con gli altri atomi adiacenti, formando delle "combinazioni" fisse che originano poi le proprietà della molecola completa.
Fra queste numerose combinazioni fisse ve n'è una particolare, questa:
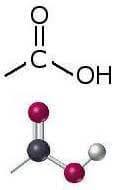
Quando questa struttura appare in una molecola la fa definire "acido carbossilico", perchè il gruppo -COOH è proprio detto "carbossile".
La lineetta iniziale indica che il gruppo carbossile deve essere attaccato a qualcos'altro, che ora non è il caso di approfondire per non complicare troppo le cose. La cosa sicura è che quando in una molecola c'è un -COOH, quella molecola è formalmente un acido (anche se non è detto che sia un "acido" come lo si intende di solito, non è "corrosivo", anzi a volte non è nemmeno "acido" al gusto).
Facciamo qualche esempio pratico:
H-COOH --> attaccato al carbossile c'è il minimo che può esserci, cioè un atomo di idrogeno.
Questo è l'acido formico (tutti gli acidi hanno una nomenclatura ufficiale, ma è molto più suggestivo questo vecchio nome tradizionale che deriva dalle formiche rosse) ed è l'acido capostipite di tutti gli altri, i quali avranno attaccato alla lineetta qualcosa di più complesso di un semplice H.
L'acido numero due? Questo tutti lo conoscono perchè è l'acido acetico, costituente fondamentale (diluito al 6%) del normale aceto da tavola, dal quale ne trae il nome. In questo caso la famosa lineetta è collegata con un gruppo -CH3 (detto "metile"), e la formula di conseguenza è CH3-COOH
Il terzo acido aggiunge al CH3- anche un -CH2- e quindi la somma totale diventa CH3-CH2-COOH e l'acido originatosi prende il nome di acido propionico (ripeto che c'è un motivo per i nomi, ma non lo dico ora).
L'appetito vien mangiando: agggiungiamo ogni volta un -CH2- in più e andiamo avanti con la catenella... CH3-CH2-CH2-COOH: ecco l'acido butirrico... CH3-(CH2)3-COOH: ecco l'acido valerico (o valerianico), e così via.
Naturalmente il carbossile può unirsi a gruppi molto più complessi di quelli appena visti, ed è ciò che origina una infinità di acidi organici, i quali però mostrano tutti una caratteristica comune: il loro bravo -COOH che spunta da qualche parte della molecola!
Termino qui questa incompletissima disanima sugli acidi organici, sperando che quell'improbabile passante al quale era rivolto questo semplice discorso non se ne sia scappato a gambe levate anzi tempo...

Inviato da: paoloalbert
il 02/05/2021 alle 21:53
Inviato da: Bepi1249
il 15/04/2021 alle 14:11
Inviato da: Tanner85
il 06/02/2021 alle 00:01
Inviato da: poetryclub
il 04/10/2020 alle 23:00
Inviato da: poetryclub
il 04/10/2020 alle 20:58