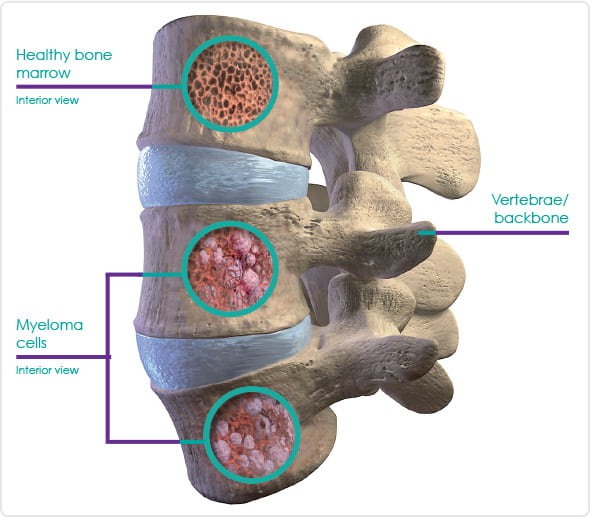
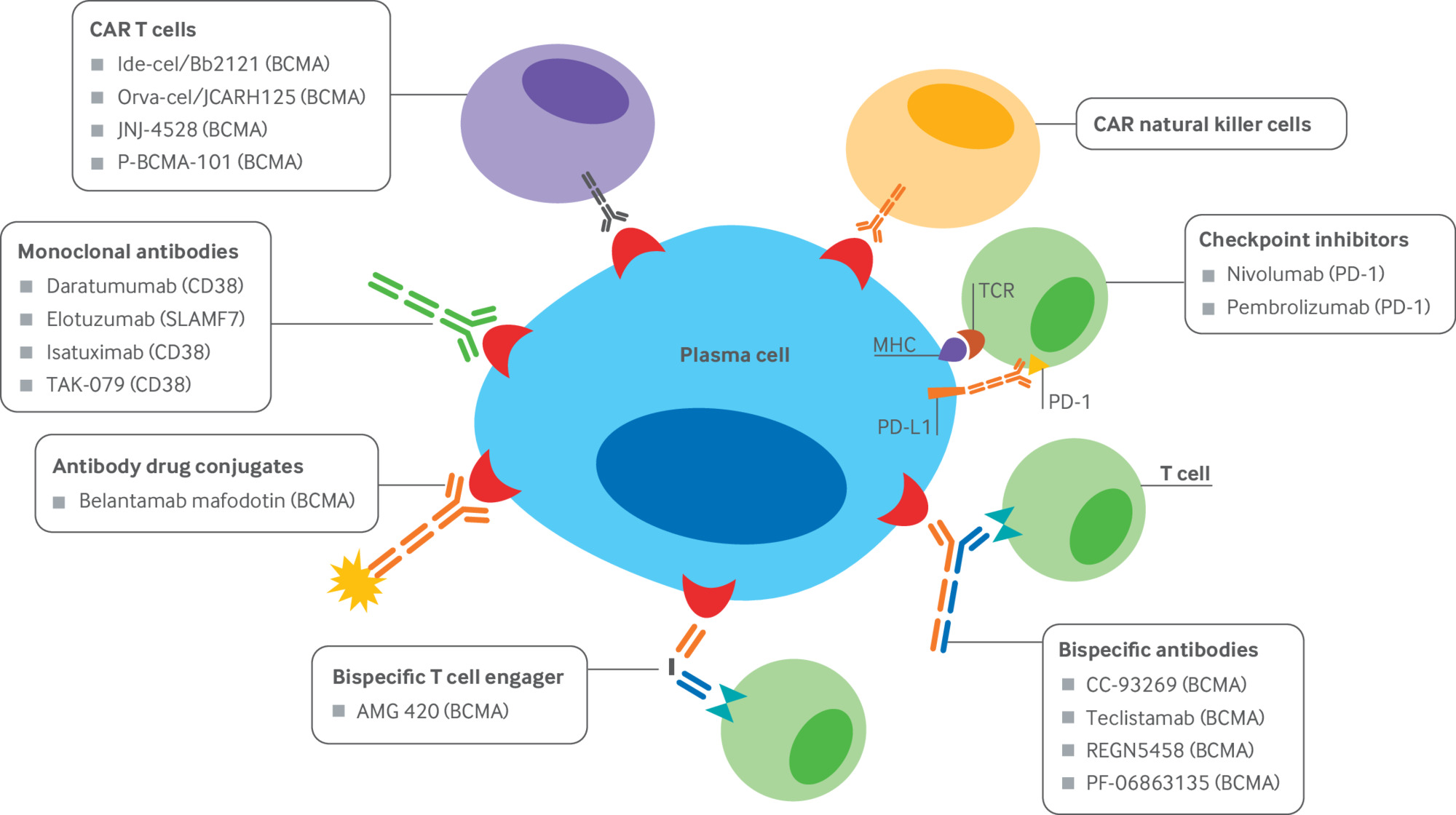
Mieloma multiplo: i bisogni insoddisfatti e le nuove terapie immuno-mediate
Quali bisogni insoddisfatti per il mieloma multiplo ?
Ci sono molte domande che devono ancora avere risposta: qual è la gestione ottimale dei pazienti ad alto rischio ? Come gestire i pazienti con fragilità significativa ? Per quanto tempo è necessario continuare il trattamento ? Quando impiegare le immunoterapie, in particolare le terapie con cellule CAR-T e gli anticorpi bispecifici ? I pazienti affetti da mieloma continuano ad avere ricadute, quali sono i meccanismi di resistenza ?
What unmet needs still exist in the multiple myeloma space as a whole ?
There are a lot of questions that still need to be asked: What is the optimal management of high-risk patients ? How do we approach patients with significant frailty ? How long do we need to continue treatment ? Where exactly do we place these immunotherapies, especially the CAR T-cell therapies and bispecifics, with a view of bringing them closer to the earlier stages of the disease ? Patients with myeloma continue to relapse, so we need to understand the mechanisms of resistance better, and a lot more needs to be learned about the biology of the disease as a whole
Aggiornamenti sulle nuove classi di terapie immuno-mirate
Elranatamab, un anticorpo bispecifico mirato a BCMA
Gli anticorpi bispecifici sembrano essere una classe di farmaci molto promettente. Promettenti sono i dati per Elranatamab, un anticorpo bispecifico mirato a BCMA, in una popolazione di pazienti pesantemente pretrattati con una mediana di 5 precedenti linee di terapia [ MagnetisMM-1 ]. Quasi l’80% di questi pazienti era refrattario di tripla classe, e i tassi di risposta erano compresi tra il 50% e il 60%, a seconda dei sottogruppi di pazienti esaminati. Nel sottogruppo di pazienti che erano stati precedentemente esposti allo stesso agente, sembra mantenere l’efficacia, anche se a un livello leggermente inferiore. La tossicità era quella prevista, con il 60-70% dei pazienti con sindrome da rilascio di citochine, nella maggior parte di grado 1 o 2. E’ stata osservata una certa tossicità ematologica, in particolare neutropenia e trombocitopenia. Non c’era tossicità neurologica significativa, ma in tutti i bispecifici, è stato riscontrato un segnale per un aumento del rischio di infezione che deve essere meglio delineato.
Talquetamab, un anticorpo bispecifico mirato a GPRC5D
Data l’esistenza di diversi agenti mirati anti-BCMA, c’è molto interesse nell’esplorare bersagli alternativi. Sono stati presentati i dati aggiornati dallo studio MonumenTAL-1 riguardante Talquetamab, un farmaco di Janssen, che è un anticorpo bispecifico mirato a GPRC5D, che ha esaminato un’ampia coorte di pazienti con malattia refrattaria, prevalentemente, a tripla classe, e anche pazienti che hanno visto più linee di terapia. Talquetamab sembra essere piuttosto attivo, con un tasso di risposta quasi del 50-60% e anche una durata della risposta abbastanza ragionevole in questa popolazione di pazienti.
Modakafusp alfa, una proteina di fusione anticorpo anti-CD38 e Interferone alfa-2b
In termini di altre terapie, sono stati presentati i dati di uno studio su Modakafusp alfa, che è un anticorpo monoclonale anti-CD38 legato a Interferone alfa-2b, in una popolazione di pazienti molto pesantemente pretrattata. Ci sono stati tassi di risposta di circa il 40% al 50%, specialmente quando si osservano sottogruppi di pazienti che non erano stati precedentemente esposti ad alcuni degli agenti più recenti, e la tossicità è apparsa essere prevalentemente ematologica.
What updates have there been in newer classes of immune-targeted therapies ?
Bispecific antibodies seem to be a very promising class of drugs. Data for Elranatamab, which is a BCMA-targeted bispecific antibody, in a heavily pretreated patient population with a median of 5 prior lines of therapy [ MagnetisMM-1 ] were presented. Nearly 80% of these patients were triple-class refractory, and the response rates were 50% to 60%, depending on the subgroups of patients they’re looking at. In the subgroup of patients who have previously been exposed to the same targeted agent, it appears to retain efficacy, albeit at a slightly lower level. The toxicity was as predicted, with 60% to 70% of patients with cytokine release syndrome. Most of them had grade 1 or 2. There was some hematological toxicity, particularly neutropenia and thrombocytopenia. There was no significant neurological toxicity, but across all bispecifics, a signal for increased risk of infection was seen.
Given that there’s a plethora of anti-BCMA targeted agents, there’s a lot of interest in exploring alternate targets. Updated data from the MonumenTAL-1 trial of Talquetamab, which is an GPRC5D-targeted bispecific, looking at a large cohort of patients with triple-class refractory disease predominantly, and also patients who have seen multiple lines of therapy. The drug seems to be quite active, with almost a 50% to 60% response rate and also a pretty reasonable durability of response given this patient population.
In terms of other therapeutics, data from a trial of Modakafusp alfa, which is an anti-CD38 targeted monoclonal antibody bound to an attenuated Interferon, in a very heavily pretreated patient population, were presented. There were response rates of about 40% to 50%, especially when you look at subgroups of patients who have previously not been exposed to some of the newer agents, and toxicity appeared to be predominantly hematologic.
Source: ASH ( American Society of Hematology ) Meeting, 2022
Xagena in Ematologia
AnemiaOnline.net | Ematologia.it | Ematologia.net | LeucemiaOnline.net | LinfomaOnline.net | Mieloma.net | TrombosiOnline.net |
Farmaci per il Mieloma multiplo
AMGEN: Kyprolis ( Carfilzomib )
BMS / CELGENE: Abecma ( Ide-Cel ) [ Terapia CAR-T anti-BCMA ]; Pomalyst ( Pomalidomide )
GSK: Blenrep ( Belantamab mafoditin )
JANSSEN: Carvykti ( Cilta-Cel; terapia CAR-T anti-BCMA ); Tecvayli ( Teclistamab, anticorpo bispecifico BCMAxCD3 ); Darzalex ( Daratumumab ) & Darzalex Faspro ( Daratumumab sottocutaneo ); Velcade ( Bortezomib )
MENARINI: Nexpovio ( Selinexor )
PFIZER: Elranatamab ( non in commercio )
SANOFI: Sarclisa ( Isatuximab; anticorpo anti-CD38 )
TAKEDA: Ninlaro ( Ixazomib )